Por José de Paiva Rebouças
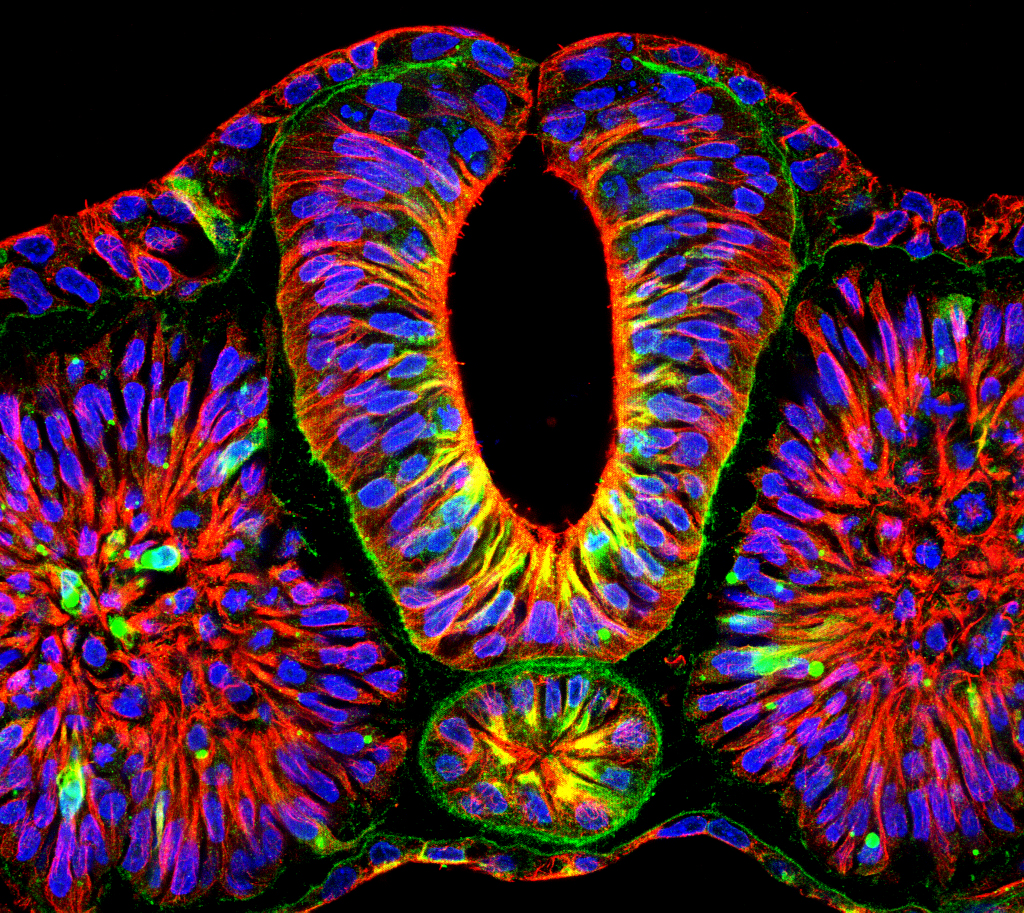
Pesquisa observou que medicamentos contra epilepsia interferem na formação do tubo neural – Elisa Martí
Pesquisa desenvolvida pelo neurocientista Eduardo Bouth Sequerra, chefe do laboratório de Desenvolvimento Neural e Ambiente do Instituto do Cérebro da Universidade Federal do Rio Grande do Norte (ICe-UFRN), descreve o mecanismo pelo qual drogas antiepilépticas induzem malformações no tubo neural. O trabalho, realizado em parceria com a pesquisadora Laura Borodinsky e publicado no último dia 30 de abril no periódico Journal of Neuroscience, abre caminhos para evitar que fetos de mulheres com epilepsia sejam prejudicados pelo uso de medicamentos para o controle da doença.
Milhões de pacientes ao redor do planeta têm suas epilepsias controladas por drogas que diminuem a atividade cerebral. As mulheres que tomam essas drogas, no entanto, têm uma maior probabilidade de gerar fetos que apresentam no dobramento e fechamento do sistema nervoso embrionário fora do padrão. Apesar dessa relação ser conhecida há muitas décadas, só a partir da pesquisa de Eduardo Sequerra é que o mecanismo molecular foi demonstrado.
“Essas drogas interferem com a atividade elétrica das células do tecido neural, uma vez que essa atividade é importante para coordenar o dobramento do tubo, induzem as malformações”, explica o neurocientista. Segundo Eduardo, isso se dá porque no início do desenvolvimento do sistema nervoso, mesmo antes de haver neurônios, as células já apresentam atividade elétrica e sinalização por neurotransmissores. Como as pacientes não podem parar de tomar a droga, acabam interferindo com o desenvolvimento do embrião.
Quando essas células se diferenciam em células neurais, iniciam uma série de alterações na sua forma. No final do ciclo, aquelas células até então organizadas como uma folha de papel se dobram até formar o tubo neural. Mais tarde, no desenvolvimento do feto, esse tubo neural vai se transformar no cérebro e na medula espinal da criança.
Acontece que pode haver falhas nesse processo, seja por mutações em alguns genes ou por fatores ambientais, como por exemplo, o uso de drogas antiepiléticas usadas por mulheres no período da gestação. “Defeitos de tubo neural podem levar à morte do embrião, como no caso de fetos anencéfalos, ou causar diversos comprometimentos àqueles que sobrevivem, como a paralisia dos membros inferiores em casos de spina bífida”, explica Sequerra.
Até então, as pesquisas nesta área estavam preocupadas em olhar para os efeitos colaterais causados pelas drogas, tentando descobrir o porquê de as moléculas inibirem o dobramento do tubo neural. Ninguém olhava para o embrião porque entendia não existir atividade elétrica no tubo neural. “Se o embrião não tem neurônios ainda, por que deveriam olhar para moléculas envolvidas na transmissão sináptica?”, questiona Eduardo que decidiu prestar atenção nesse detalhe.
Pesquisador do ICe-UFRN, Eduardo Sequerra, investigou quando começavam as atividades elétricas no tubo neural – Acervo Eduardo Sequerra
O neurocientista observou que o sistema nervoso já apresenta sinais de atividade elétrica muito antes de formar suas sinapses ou até ter neurônios diferenciados, o problema é que não sabíamos o quão cedo isso começava. Este, então, foi o pontapé que ele precisava para iniciar sua pesquisa.
Atividade elétrica no tubo neural
A pesquisa de Eduardo Sequerra foi realizada no laboratório de Laura Borodindinsky, na University of California, em Davis (EUA). Na época, Laura estava iniciando a formação do seu grupo que estuda o desenvolvimento em embriões do sapo Xenopus laevis. Por se desenvolverem fora da mãe, esses anfíbios são perfeitos como modelo animal para este tipo de investigação.
Os pesquisadores observaram que as células da placa neural (as células neurais ainda organizadas em forma de folha, antes de dobrar) expressavam receptores para diversos neurotransmissores. Estas células, segundo Eduardo, também produzem grandes entradas do íon cálcio em seu citoplasma, mostrando uma atividade elétrica primitiva.
A partir disso, a pesquisa passou a concentrar em um receptor do neurotransmissor glutamato, muito encontrado em neurônios jovens, o receptor N-metil D-Aspartato (rNMDA). “Se inibirmos esse receptor com um inibidor específico ou inibindo a tradução do seu RNA mensageiro, os embriões formam defeitos de tubo neural”, disse o pesquisador.
Percebido isso, os investigadores sabiam que os alvos utilizados pelas drogas antiepilépticas para controlar as epilepsias no cérebro adulto também estão presentes durante o dobramento do tubo neural. “Percebemos que se inibirmos esta sinalização temos um efeito muito parecido ao das drogas que causam a indução de defeitos de tubo neural”, adiantou Sequerra.
Faltava agora mostrar que as drogas antiepilépticas induziam defeitos de tubo neural através da inibição do rNMDA. Apesar dos fortes indícios de que as duas coisas estavam ligadas, ainda havia a possibilidade de as drogas antiepilépticas interferirem com o dobramento do tubo neural por outro mecanismo independente de neurotransmissores. E é aí que entraram os experimentos de resgate.
Nesta etapa, os pesquisadores trataram de recuperar a formação do tubo neural na presença do ácido valpróico (VPA, uma droga antiepiléptica amplamente utilizada) através da recuperação da sinalização pelo rNMDA. “Se incubarmos os embriões com VPA e um excesso de NMDA (que ativa o receptor) aumentamos o número de influxos de cálcio”, informou Eduardo.

Embriões do sapo Xenopus laevis foram utilizados como modelo animal para o desenvolvimento da pesquisa – Acervo Eduardo Sequerra
Além disso, foi percebido que estes embriões fazem defeitos de tubo neural menos extensos. “Se ativarmos artificialmente a enzima intracelular (chamada MEK), que naturalmente o rNMDA só ativaria quando o glutamato se ligasse, a mesma redução na extensão dos defeitos acontece”, completou.
Alerta
A pesquisa mostrou que estes experimentos produzem um resgate parcial do dobramento do tubo neural, o que sugere haver um balanço na ativação das moléculas manipuladas. O estudo sugere ainda que podem haver outros alvos das drogas que contribuam para a regulação da formação do tubo neural.
No artigo publicado no Journal of Neuroscience, Eduardo Sequerra demonstra que não é seguro interferir com a sinalização pelo receptor tipo NMDA durante o dobramento do tubo neural, o que cria um alerta sobre a utilização das drogas durante as semanas iniciais da gestão. Isso, segundo o pesquisador, é vital para coordenar fenômenos como a divisão celular e a migração de diversas células durante o dobramento de todo o tecido.








